Yuanfeng POV: cronologia aggiornata dell'EUDAMED
La Commissione europea ha recentemente annunciato aggiornamenti per completare e attuare EUDAMED sulla base dell'emendamento 2024/1860.Questo articolo illustra gli attuali tempi di EUDAMED e il nostro punto di vista su questi tempi per aiutare l'industria a prepararsi di conseguenza.
Timeline attuale dell'EUDAMED:
- La data di riferimento per la prima applicazione obbligatoria dei moduli funzionali EUDAMED è ancora il 1o gennaio 2026.Il modulo di vigilanza dovrebbe essere obbligatorio a partire dal terzo trimestre del 2026, con la piena funzionalità EUDAMED prevista per il secondo trimestre del 2027..
- I moduli Actor, UDI & Devices, Certificati e Sorveglianza del mercato sono attualmente in fase di audit.L'audit indipendente del prodotto minimo vitale (MVP) ha lo scopo di valutare e confermare la funzionalità e l'interconnettività dei moduli ritenuti pronti per l'auditTale audit dovrebbe essere completato entro il secondo trimestre del 2025.
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)L'Actor, UDI & Devices, Certificati e moduli di vigilanza del mercato dovrebbero essere dichiarati pienamente funzionali alla fine del secondo trimestre 2025, portando alla loro data di applicazione obbligatoria del 1° gennaio. 2026.
- Sì. - I moduli Actor, UDI & Devices, Certificates e Market Surveillance dovrebbero essere dichiarati pienamente funzionali entro la fine del secondo trimestre 2025 e obbligatori per l'uso industriale il 1o gennaio 2026.
- Il modulo di vigilanza non fa parte dell'audit MVP in corso e non sarà dichiarato pienamente funzionale insieme ai moduli precedentemente menzionati.Il calendario rivisto indica che l'audit di tale modulo si svolgerà tra il secondo e il terzo trimestre del 2025, con l'obiettivo della data di applicazione obbligatoria nel secondo trimestre del 2026.
- Sì. - Lo sviluppo del modulo di indagine clinica/studi sulle prestazioni (CI/PS) dovrebbe continuare fino al terzo trimestre 2026.Una revisione per valutare il modulo CI/PS insieme agli altri cinque (5) moduli sarà completata una volta sviluppato il MVP CI/PS.
- Sì.
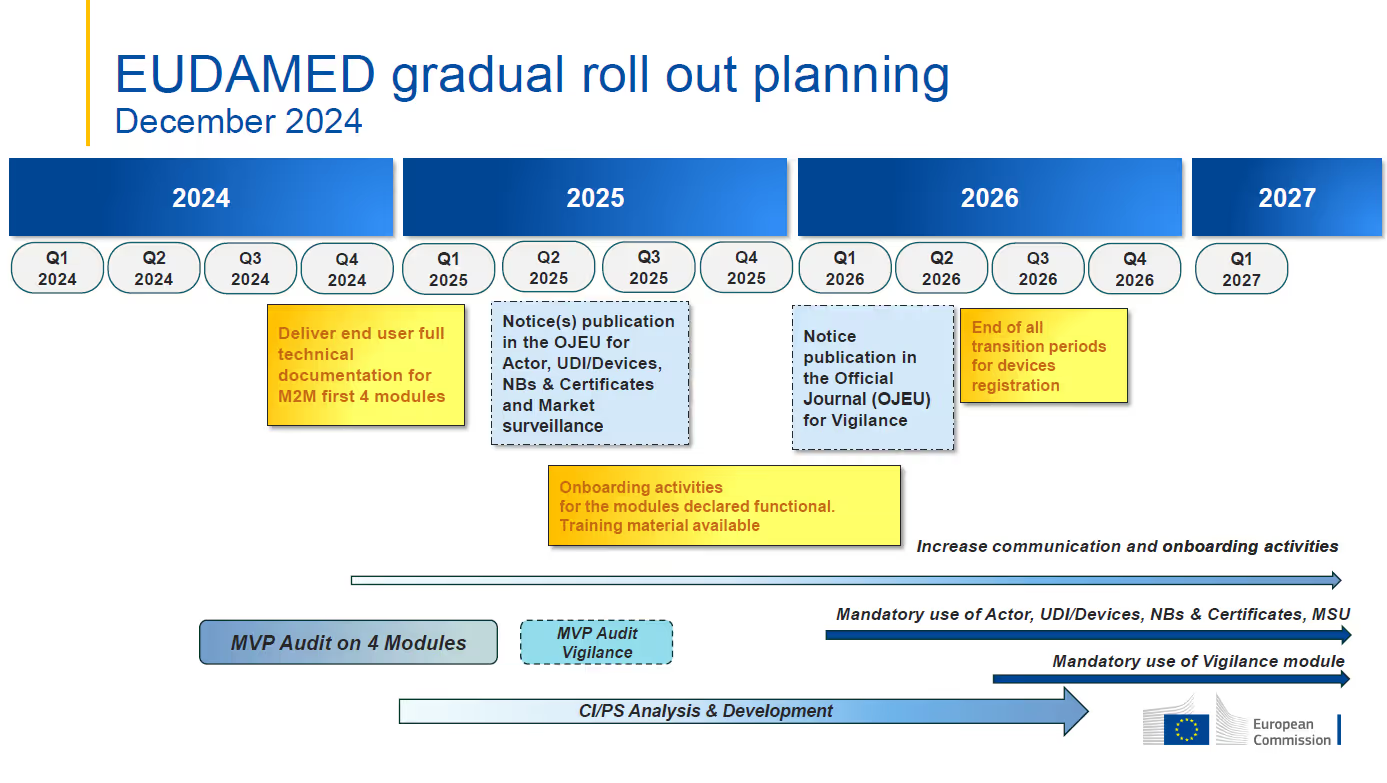
Foto con la cortesia delCommissione europea
La Commissione europea ha recentemente annunciato aggiornamenti per completare e attuare EUDAMED basati su:modifica 2024/1860.Questo articolo illustra gli attuali tempi di EUDAMED e il nostro punto di vista su questi tempi per aiutare l'industria a prepararsi di conseguenza.
Timeline attuale dell'EUDAMED:
- La data di riferimento per la prima applicazione obbligatoria dei moduli funzionali EUDAMED è ancora il 1o gennaio 2026.Il modulo di vigilanza dovrebbe essere obbligatorio a partire dal terzo trimestre del 2026, con la piena funzionalità EUDAMED prevista per il secondo trimestre del 2027..
- I moduli Actor, UDI & Devices, Certificati e Sorveglianza del mercato sono attualmente in fase di audit.L'audit indipendente del prodotto minimo vitale (MVP) ha lo scopo di valutare e confermare la funzionalità e l'interconnettività dei moduli ritenuti pronti per l'auditTale audit dovrebbe essere completato entro il secondo trimestre del 2025.
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)L'Actor, UDI & Devices, Certificati e moduli di vigilanza del mercato dovrebbero essere dichiarati pienamente funzionali alla fine del secondo trimestre 2025, portando alla loro data di applicazione obbligatoria del 1° gennaio. 2026.
- Sì. - I moduli Actor, UDI & Devices, Certificates e Market Surveillance dovrebbero essere dichiarati pienamente funzionali entro la fine del secondo trimestre 2025 e obbligatori per l'uso industriale il 1o gennaio 2026.
- Il modulo di vigilanza non fa parte dell'audit MVP in corso e non sarà dichiarato pienamente funzionale insieme ai moduli precedentemente menzionati.Il calendario rivisto indica che l'audit di tale modulo si svolgerà tra il secondo e il terzo trimestre del 2025, con l'obiettivo della data di applicazione obbligatoria nel secondo trimestre del 2026.
- Sì. - Lo sviluppo del modulo di indagine clinica/studi sulle prestazioni (CI/PS) dovrebbe continuare fino al terzo trimestre 2026.Una revisione per valutare il modulo CI/PS insieme agli altri cinque (5) moduli sarà completata una volta sviluppato il MVP CI/PS.
- Sì.

Foto con la cortesia delCommissione europea
Ecco come Rimsys vede l'impatto di questo annuncio per ciascun gruppo di parti interessate:
Yuanfeng
L'UDI è al centro della nostra attenzione, così come le future interazioni con il modulo di vigilanza.Rimsys continuerà a sviluppare la funzionalità UDI e la funzionalità di vigilanza post-mercato indipendentemente dalle date di riferimento aggiornateRiconosciamo inoltre il potenziale impatto dell'istituzione di capacità di trasferimento di dati (DTX) per interagire con EUDAMED in una capacità di macchina a macchina (M2M).Con la pubblicazione dei requisiti definitivi necessari per il M2M DTX all'EUDAMED, Rimsys è posizionata per finalizzare la nostra connessione e fornire capacità M2M come parte della soluzione EUDAMED.
Industria/cliente
Dato che la Commissione europea ha effettuato numerosi aggiornamenti dei tempi di EUDAMED, ci aspettiamo che l'industria abbia qualche riluttanza ad accettare le nuove date di riferimento.Questo potrebbe ritardare il ri-impegno con i preparativi dell'EUDAMEDTuttavia, non ci aspettiamo che la CE spinga questi tempi aggiornati.I produttori che non hanno in programma di presentare dati all'EUDAMED entro il secondo trimestre di quest'anno dovrebbero aspettarsi sfide significative per rispettare questi terminiCon l'audit dei moduli attesi in corso e la relativa documentazione tecnica pubblicata,Rimsys raccomanda di prendere provvedimenti per organizzare i dati normativi ora e di trasmettere tempestivamente le loro informazioni a tutti i moduli EUDAMED disponibili.
Commissione dell'UE
La CE raccomanda vivamente all'industria di continuare a sviluppare la propria soluzione e di presentare dati su base volontaria.La posizione della Commissione è che la presentazione precoce dei dati darà alle imprese un vantaggio in quanto i loro dati saranno disponibili prima dell'attacco di tutta l'industria medica globale., tutte le imprese che cercano di aggiungere dati allo stesso tempo EUDAMED diventa obbligatorio.
* Nota: questo articolo comprende interpretazioni e pareri regolamentariYuanfengIl nostro team cerca di essere il più informativo possibile, ma queste informazioni non sono destinate a sostituire le indicazioni ufficiali delle autorità di regolamentazione.

